
Allergische Immunantworten helfen bei der Abwehr bakterieller Infektionen
AllgemeinGesundheitsnewsStudien 19. März 2021 Dr. Polwin-Plass Lydia

Eine gemeinsame Studie des CeMM Forschungszentrums für Molekulare Medizin der Österreichischen Akademie der Wissenschaften, der Medizinischen Universität Wien und der Stanford University School of Medicine vom Herbst 2020 könnte erklären, warum der Körper im Laufe der Evolution an einem bekannten „Allergiemodul“ festgehalten hat. Dieser Baustein des Immunsystems, bestehend aus Mastzellen und Immunglobolin E (IgE) Antikörpern, kann die Widerstandskraft des Körpers gegen sekundäre bakterielle Infektionen erhöhen.
Die Studie leistet einen wichtigen Beitrag zum allgemeinen Verständnis des Immunsystems und wurden im renommierten Fachjournal Immunity veröffentlicht.
Rund 150 Millionen EuropäerInnen leiden unter wiederkehrenden Allergien. Laut einer Studie der europäischen Akademie für Allergologie und klinische Immunologie könnte bis 2025 jede(r) zweite EuropäerIn von einer Allergie betroffen sein.
Allergische PatientInnen durchlaufen zu Beginn der Erkrankung einen Prozess der „Sensibilisierung“. Dabei entwickelt ihr Immunsystem IgE-Antikörper, die körperfremde Stoffe, sogenannte Allergene erkennen. Die IgE Antikörper wiederum binden an Zellen mit einem FcεR1 Rezeptor, der vor allem auf Mastzellen, einer Art Immunzelle vorkommt, die in den meisten Geweben des Körpers vorhanden sind. Bei erneutem Kontakt mit einem Allergen vermitteln die IgE-Antikörper die sofortige Aktivierung der Mastzellen und die unmittelbare Freisetzung verschiedener Mediatoren, z.B. Histamin, Proteasen oder verschiedene Zytokine, welche die klassischen allergischen Symptomen hervorrufen.
Abhängig vom Organ, in dem es zum Kontakt mit dem Allergen kommt, können die Symptome von Niesen/Atemnot (Atemwege) über Durchfall und Magenschmerzen (Magen-Darm-Trakt) bis hin zu Juckreiz (Haut) reichen. Systemischer Kontakt mit Allergenen, zum Beispiel durch Erreichen des Blutkreislaufs, kann zur gleichzeitigen Aktivierung einer großen Anzahl von Mastzellen in verschiedenen Organen führen, was eine Anaphylaxie – eine schwerwiegende, lebensbedrohliche allergische Reaktion – hervorrufen kann.
Trotz langjähriger Forschung an IgE-Antikörpern und Mastzellen konnte die biologische Funktion dieses „Allergiemoduls“ bis heute noch nicht vollständig geklärt werden. Bereits 1991 postulierte Margie Profet in ihrer „Toxin-Hypothese“ eine positive Funktion allergischer Reaktionen bei der Abwehr von Giftstoffen.
Frühere Studien von Stephen J. Galli, Senior Co-Autor der aktuellen Publikation an der Stanford University haben diese These untermauert und die Bedeutung von Mastzellen für die angeborene Resistenz gegen das Gift bestimmter Schlangen und der Honigbiene beschrieben, bzw. unter Mitwirkung von Erstautor Philipp Starkl, deren Relevanz im Zusammenspiel mit IgE-Antikörpern für die erworbene Immunabwehr gegen große Giftmengen aufgezeigt.
Auf Basis dieser Erkenntnisse untersuchten Philipp Starkl, Senior Postdoc an der Meduni Wien und CeMM, zusammen mit Sylvia Knapp, Professorin an der MedUni Wien und CeMM PI, sowie Stephen J. Galli, Professor an der Stanford University School of Medicine, und KollegInnen in der aktuellen Studie, ob Mastzellen und IgE-Antikörper auch bei der Abwehr anderer toxinproduzierender Organismen, insbesondere pathogener Bakterien, relevant sein könnten. Wegen seiner enormen klinischen Relevanz und seines breiten Repertoires an Toxinen wählten die AutorInnen das Bakterium Staphylococcus aureus als Erregermodell. Staphylococcus aureus ist ein typischer antibiotikaresistenter Krankheitserreger und wird auch mit der Entwicklung allergischer Erkrankungen wie Asthma und atopische Dermatitis in Verbindung gebracht. Für ihre Forschung verwendeten die WissenschaftlerInnen verschiedene S. aureus-Mausinfektionsmodelle in Kombination mit genetischen Ansätzen und In-vitro-Mastzellmodellen, um die Funktionen ausgewählter Komponenten der IgE-Effektormechanismen zu entschlüsseln.
Die wissenschaftliche Untersuchung deutete darauf hin, dass die „allergische“ Immunantwort nicht ausschließlich pathologisch, sondern schützend bei bakteriellen Infektionen sein kann. Die Abwehr von toxinproduzierenden pathogenen Bakterien könnte daher eine wichtige biologische Funktion des „Allergiemoduls“ sein.
Die spannende Entdeckung trägt nicht nur zum besseren allgemeinen Verständnis des Immunsystems und vor allem allergischer Immunreaktionen bei, sondern könnte auch miterklären, warum der Körper im Laufe der Evolution am „Allergiemodul“ festgehalten hat. Denn trotz ihrer gefährlichen Rolle bei allergischen Erkrankungen können IgE-Antikörper und Mastzellen positive Funktionen ausüben, die mithelfen, den Körper gegen Gifte und Infektionen durch toxinproduzierende Bakterien wie S. aureus zu schützen.
Diese Studie stellt eine wichtige Kooperation dar, die von Philipp Starkl im Labor von Stephen J. Galli an der Stanford University zusammen mit anderen Kollegen initiiert und danach im Labor von Sylvia Knapp an der Medizinischen Universität Wien und am CeMM fortgesetzt wurde.
Quelle: Europäische Akademie für Allergologie und klinische Immunologie (EAACI, 2016)
Science. 2006 Jul 28;313(5786):526-30. DOI: 10.1126/science.1128877
Immunity. 2013 Nov 14;39(5):963-75. doi: 10.1016/j.immuni.2013.10.005
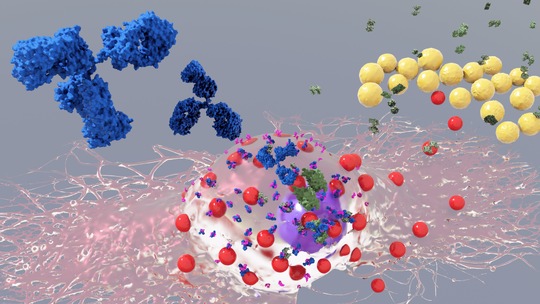
Headerbild: Künstlerische 3D Darstellung einer Mastzelle (Bildmitte) mit IgE Antikörpern (in blau; gebunden an den FceRI Rezeptor, in rosa, auf der Zelloberfläche) und Staphylococcus aureus Bakterien (in gold). (© Bobby R. Malhotra / CeMM)
Die Studie „IgE Effector Mechanisms, in Concert with Mast Cells, Contribute to Acquired Host Defense against Staphylococcus aureus“ wurde am 9. September 2020 in der Fachzeitschrift „Immunity“ veröffentlicht. DOI: DOI: 10.1016/j.immuni.2020.08.002
AutorInnen: Philipp Starkl, Martin L. Watzenboeck, Lauren M. Popov, Sophie Zahalka, Anastasiya Hladik, Karin Lakovits, Mariem Radhouani, Arvand Haschemi, Thomas Marichal, Laurent L. Reber, Nicolas Gaudenzio, Riccardo Sibilano, Lukas Stulik, Frédéric Fontaine, André C. Mueller, Manuel R. Amieva, Stephen J. Galli*, Sylvia Knapp* | * Senior-Co-AutorInnen
Finanzierung: Die Studie wurde vom Österreichischen Wissenschaftsfonds (FWF J3399-B21) und durch NIH-Mittel (R01 AI23990, R01 AI070813, R01 AR067145 und R01 AI132494) unterstützt (an Stephen J. Galli). Philipp Starkl wurde durch ein Marie Skłodowska-Curie Individual Fellowship (H2020-MSCA-IF-2014 Nr. 655153), den Österreichischen Wissenschaftsfonds (FWF P31113-B30) und ein Schrödinger-Stipendium des FWF unterstützt (J3399-B21).
Sylvia Knapp, MD, PhD, ist Professorin für Infektionsbiologie an der Medizinischen Universität Wien.
Das CeMM Forschungszentrum für Molekulare Medizin der Österreichischen Akademie der Wissenschaften ist eine internationale, unabhängige und interdisziplinäre Forschungseinrichtung für molekulare Medizin unter der wissenschaftlichen Leitung von Giulio Superti-Furga. www.cemm.oeaw.ac.at