
Ein adaptierter Wirkstoff könnte als Prophylaxe gegen Magenkrebs wirken
AllgemeinGesundheitsnewsStudien 18. März 2026 Dr. Polwin-Plass Lydia

Forschende der TUM haben einen vielversprechenden Fortschritt im Kampf gegen das weit verbreitete Bakterium Helicobacter pylori gemacht. Durch gezielte chemische Adaptierung eines bekannten Antibiotikums gelang es ihnen, dessen Wirksamkeit um das 60-Fache zu steigern. Es könnte langfristig helfen, Magengeschwüre und als Folge davon auch Magenkrebs zu verhindern.
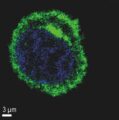
Helicobacter pylori ist weltweit verbreitet und kann chronische Entzündungen der Magenschleimhaut und in Folge Magengeschwüre oder sogar Magenkrebs verursachen. Rund 43 Prozent der Bevölkerung tragen den Keim in sich. Die bisher eingesetzten Therapien stoßen jedoch zunehmend an ihre Grenzen, da das Bakterium immer häufiger Resistenzen entwickelt.
Das Forschungsteam um Prof. Stephan A. Sieber untersuchte den Wirkmechanismus des Standardantibiotikums Metronidazol genauer und entdeckte dabei neue Angriffspunkte im Bakterium. Aufbauend auf diesen Erkenntnissen entwickelten sie modifizierte Varianten des Wirkstoffs, sogenannte Ether-Derivate. Diese binden stabiler an zentrale Schutzproteine von Helicobacter pylori und schwächen so dessen Abwehrmechanismen deutlich.
Die Ergebnisse sind vielversprechend – in Labor- und Tierversuchen zeigte der neue Wirkstoff eine deutlich erhöhte Wirksamkeit – auch gegen resistente Bakterienstämme. Gleichzeitig blieb die Verträglichkeit für menschliche Zellen unverändert. In Versuchen an Mäusen konnte die Infektion sogar vollständig beseitigt werden, und das bei geringerer Dosierung und mit weniger Auswirkungen auf das Darmmikrobiom.
Trotz dieser Erfolge steht ein entscheidender Schritt noch aus: Klinische Studien am Menschen. Sollten sich die Ergebnisse bestätigen, könnte der adaptierte Wirkstoff nicht nur die Behandlung von Helicobacter pylori-Infektionen verbessern, sie könnten auch einen wichtigen Beitrag zur Vorbeugung von Magenkrebs leisten.
Headerbild: Helicobacter pylori: Raquel Mejías Luque / TUM